
불로장생의 길을 여는 열쇠
텔로미어
- 325호
- 기사입력 2015.06.13
- 취재 김나현 기자
- 편집 김혜린 기자
- 조회수 11884

불로장생(不老長生)하면 무엇이 떠오르는가? 고대 중국을 통일한 첫 번째 진시황(秦始皇)제는 불로장생의 아이콘이라 할 수 있다. 먹으면 영원히 죽지 않는 불로초(不老草)를 구해오도록 한 것은 진시황의 야망을 알 수 있는 대목이다. 과연 진시황만이 불로장생에 대한 욕망을 가졌던 걸까? 불로장생(不老長生), 또는 불로불사(不老不死)를 향한 욕망이 발현된 흔적은 어디에서나 찾아볼 수 있다. 신화나 민간 문학작품에서 심심치 않게 등장하는 불로(不老)의 영약이 그것이다. 현대에서는 ‘벤자민 버튼의 시간은 거꾸로 간다’ 등등, 노인이 회춘해서 겪는 에피소드를 담은 문화콘텐츠들이 등장한다. 첨단과학을 달리는 21세기에도 ‘젊음’과 ‘무병장수’에 대한 욕망이 살아있는 것이다. 그러던중 2009년 드디어 그 욕망에 대한 실마리를 얻게 된다.
2009년 노벨상 생리의학부문 수상자는 엘리자베스 H. 블랙번, 캐럴 W. 그라이더, 잭 W. 조스택 박사이다. 이들의 공통된 키워드는 바로 ‘텔로미어’이다. 이 생소한 물질의 규명으로 우리는 세포의 ‘노화’에 대한 비밀을 알게 됐다. 과연 그들이 밝힌 현대판 불로장생(不老長生)의 열쇠, 텔로미어란 무엇일까?

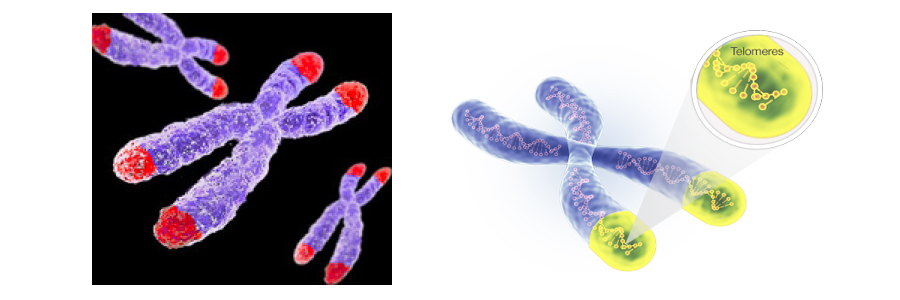
사진출처 – www.psychologytoday.com, www.tasciences.com
인간은 총 수십조 개의 체세포로 이루어져 있다. 수정란 때부터 시작되는 세포분열은 인간이 태어나고 죽을 때까지 계속된다. 세포분열은 하나의 새로운 세포를 ‘복제’하는 과정으로, 먼저 생명체의 유전정보를 완벽하게 복제한 뒤 세포가 둘로 쪼개지게 된다. 하지만 이 과정 속에서 흥미로운 사실을 발견한다. 세포가 분열할 때마다 유전정보를 담고 있는 염색체의 길이가 조금씩 짧아지는 것이다. 이런 현상을 발견한 생물학자는 DNA의 이중나선구조를 발견한 왓슨, 크릭 박사들이다. 사람의 유전정보는 DNA의 염기서열로 염색체 안에 존재하나, 만약 염색체에 이상이 생기면 만들어지는 세포는 비정상이 된다. 그러나 하루에도 수없이 많은 세포분열을 거듭하는 우리들은 특별한 이상이 생기지 않는다. 그렇다면 세포분열 때마다 잃어버리는 염색체의 끝부분은 도대체 어떤 유전정보가 있기에 잘려나가도 우리는 아무 이상이 없는 것일까?
답은 1970년대에 와서 드러났다. 염색체 끝부분쯤에서 반복되는 DNA염기서열은 다른 부분보다 특별했다. 1946년 노벨상을 수상한 멀러 박사는 이 부분을 그리스어로 ‘끝’을 의미하는 Telos와 ‘부분’을 의미하는 Meros를 연결하여 ‘텔로미어’(Telomere)라 이름지었다. 텔로미어는 6개의 뉴클레오티드(AATCCC, TTAGGG 등)가 수천번 반복적으로 나열된 염기서열과 여기에 결합하는 단백질의 복합체이다. 이 텔로미어는 세포 분열을 거듭할때마다 조금씩 잘려나가는 데 그럼에도 불구하고 우리가 세포의 이상 없이 정상적인 이유는 텔로미어 속에는 중요한 유전정보가 담겨있지 않기 때문이다. 있어도 그만 없어도 그만인 듯한 이 부분이 어떤 역할을 하는 것일까?


사진출처 – writedirection.com
텔로미어의 역할을 비유할 때 흔히 ‘구두끈 끝에 달려있는 플라스틱 캡’, 또는 ‘밧줄 속 새끼끈이 풀리지 않게 묶는 매듭’에 비유한다. 그 이유는 텔로미어는 세포분열 시 염색체가 풀어지지 않게 막아주며, 그 과정에서 염색체와 DNA가 닳아 없어지지 않게 막아주는 역할을 맡기 때문이다. 한마디로 염색체를 보호하는 기능을 한다. 텔로미어는 다른 중요한 유전정보를 담고 있는 염색체보다 끝단에 위치하여 세포분열시 오는 손상을 대신 받아 정상세포를 만들 수 있는 것이다.
세포분열하면서 사람의 염색체는 필연적으로 짧아지게 된다. 따라서 텔로미어는 세포분열을 거듭하다보면 일정길이 이하로 짧아지게 되는 당연한 현상이 일어난다. 그렇다면 그때 세포는 어떻게 되는 것일까? 일반적으로 약 60~70차례의 세포분열을 거친 세포는 세포분열을 멈추고 사멸하기만을 기다린다. 이 세포분열 한도를 ‘헤이플릭 한계’라고 부르는데 1960년대에는 그 원인을 명확히 밝히지 못했다. 하지만 후에 헤이플릭 한계는 텔로미어의 길이가 노화점 아래로 짧아짐으로 세포가 ‘노화’상태에 빠져 세포분열을 멈추는 것을 의미한다는 것이 밝혀졌다. 텔로미어는 일정길이 이하로 짧아질 때 세포의 성장을 멈추고 노화상태로 도달하게 하는 ‘생체타이머’의 역할도 맡는다고 할 수 있다. 이처럼 텔로미어는 ‘노화’와 직접적인 관계가 있다는 것이 드러났다.

텔로미어가 ‘노화’와의 연관성을 보여주는 다른 예는 바로 ‘선천성 조로증(早老症)’환자들의 텔로미어이다. 그들은 태어날 때부터 정상인들보다 짧은 텔로미어를 가진 채로 태어나기 때문에 노화가 굉장히 일찍 찾아온다. 다시 말해 짧은 텔로미어는 곧 세포의 ‘노화’를 진행시키는 중요한 원인중 하나이다. 이것이 초래하는 세포의 노화상태는 여러 가지 부정적인 결과를 낳는다. 대표적으로 노인들이 많이 겪는 동맥경화, 감각기관기능저하, 상처회복 및 면역 능력 약화 등의 질병이 그것이다. 위에서 언급했다시피 인간은 평생동안 각 세포들이 세포분열을 거듭한다. 즉 텔로미어가 짧아지는 것은 필연적인 것이다. 하지만, 만약 ‘노화’의 잣대가 되는 텔로미어의 길이가 길어진다면 ‘노화’를 막을 수 있는 것일까?

사진출처 - 네이버
2009년 노벨생리의학상을 수상받은 3명의 학자들이 연구한 내용은 다음과 같다. 첫 째, 텔로미어의 유전자 구조 규명과 그 기능 연구. 둘 째, 염색체의 DNA가 복제될 때 짧아지지 않는 세포들의 이유를 찾은 것이다. 일반적인 세포들은 텔로미어가 태아 때 만들어질 때가 가장 길며 그 이후는 분열을 거듭해 조금씩 잘려나간다. 하지만 예외인 세포들이 존재한다. 그 예들은 바로 생식세포, 조혈모세포, 암세포가 그것이다.
특히 암세포는 무한히 세포분열을 해 걷잡을 수 없이 커진 세포덩이들을 의미한다. 암세포는 끊임없이 세포분열을 해도 텔로미어가 짧아지지 않는다. 여기에서 밝혀진 이유는 바로 암세포의 ‘텔로머라아제(Telomerase)’가 활성화됐기 때문이다. 텔로머라아제는 일반 염색체 말단에 위치하며 텔로미어를 만들어내는 효소이다. 일반 세포들도 모두 이 텔로머라아제의 유전자를 가지고 있지만 ‘비활성’상태로 일반적인 세포는 텔로미어가 길어지지 않는다. 하지만 정상적인 세포 가운데 텔로머라아제가 활성화된 세포는 생식세포나 혈구를 만들어내는 조혈모세포 등이 있다.
생식세포의 텔로미어가 분열을 거듭해 짧아져 노화가 오게 된다면 더 이상 생식을 할 수 없게 되는 것은 물론이다. 생식세포의 텔로머라아제가 활성화 돼 텔로미어가 길게 보존되는 것은 ‘노인’이 태어나지 않는 이유가 되는 것이다. 혈구를 만들어내는 조혈모세포도 마찬가지이다. 조혈모세포가 텔로미어가 짧아져 분열이 정지된다면 인간은 유한한 혈구만을 가지고 짧은 생을 살 수 밖에 없을 것이다. 텔로머라아제가 비정상적으로 활성화된 예시는 위에서 언급한 암세포이다. 2009년 3명의 생물학자가 밝혀낸 이 ‘텔로머라아제’는 실로 의학계에 굉장한 파문을 불러일으켰다. 암을 치료할 때 이 텔로머라아제를 억제하는 방향으로 진행한다면 암세포의 증식을 막아 쉬운 치료가 가능해질 것이기 때문이다. 그리고 ‘노화’에 큰 영향을 끼치는 텔로미어의 길이를 늘림으로써 불로장생(不老長生)이 한 발짝 더 가시화됐기 때문이다.
일반세포속의 텔로머라아제 유전자를 활성화시켜 필요할 때마다 텔로미어를 연장하게 되면 이론상 세포는 늙지 않을 것이다. 현재 이런 약이 개발 중에 있으나 여전히 부작용이 우려되는 시점이기에 아직 갈 길은 멀다.
참조 – 노벨상이 찾아낸 불로장생의 비밀, 텔로미어. 마이클 포셀 외 지음| No. | 제목 | 등록일 | 조회 |
|---|---|---|---|
| 10 | 329호 자본주의 거품경제의 시초 튤립투기(Tulip Mania) | 2015-08-13 | 13525 |
| 9 | 327호 허가받은 약탈자, 사략선 | 2015-07-13 | 12860 |
| 8 | 325호 불로장생의 길을 여는 열쇠 텔로미어 | 2015-06-13 | 11884 |
| 7 | 323호 해장 - 건강하게 술 먹기 | 2015-05-12 | 12019 |
| 6 | 321호 신께서 허락한 음식, 할랄(Halal Food) | 2015-04-13 | 13564 |
| 5 | 319호 푸앵카레의 추측 - 100년만에 풀린 난제 | 2015-03-13 | 15762 |
| 4 | 317호 클레이 수학 연구소 - 세계 7대 난제의 탄생 | 2015-02-11 | 15050 |
| 3 | 315호 자유로운 입국을 위한 허가증, VISA | 2015-01-13 | 12114 |
| 2 | 200호 단비의 1년! | 2010-03-18 | 4554 |
| 1 | 100호 내 몸안에 또 다른 누군가가 있다면? - Chimera, 그리고 Chimera Placity | 2006-01-14 | 7285 |

